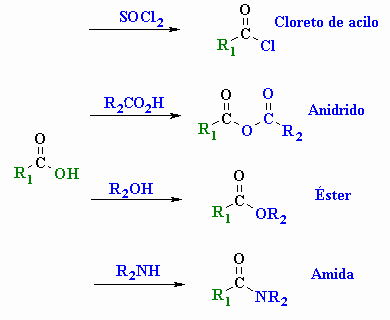
Figura 1 - Derivados de ácidos carboxílicos.
Tópico 49- Derivados de
ácidos carboxílicos
Na figura 1 são indicadas algumas reacções
típicas dos ácidos carboxílicos em que ocorre
substituição do grupo hidroxilo ou do oxigénio do
grupo hidroxilo por outro grupo substituinte dando origem a diferentes
famílias de compostos.

Figura 1 - Derivados de ácidos carboxílicos.
Em todos os derivados de ácidos carboxílicos é conservado o grupo R1C(O) e o carbono estabelece uma ligação σ com o átomo apropriado do grupo substituinte respectivo, indicados a azul na figura 1. Neste grupo, o carbono e oxigénio estão rodeados de três zonas com electrões e apresentam assim hibridação sp2 e configurações:
carbono [He] 2sp212sp21sp212pz1
oxigénio [He] 2sp222sp22sp212pz1
O carbono do grupo carbonilo estabelece 3 ligações σ com as orbitais sp2, uma com uma orbital do grupo substituinte, outra com uma orbital do átomo do radical R a que se liga, e uma terceira ligação σ com uma orbital sp2 do oxigénio do grupo C=O. Este último apresenta as restantes orbitais sp2 ocupadas com dois pares de electrões não partilhados. As orbitais pz do carbono e oxigénio do grupo carbonilo que não entraram na hibridação coalescem lateralmente estabelecendo uma ligação π.
Cloretos
de acilo
Os cloretos de acilo são compostos de fórmula geral fórmula geral RCOCl. A nomenclatura destes compostos consiste em designá-los por cloretos do ácido correspondente com terminação ilo. O derivado do ácido acético designa-se assim cloreto de acetilo. Na figura 2 são descritas a ligação neste composto e é representada a superfície de densidade electrónica. O cloreto de acetilo, assim como os restantes compostos desta família, apresenta um momento dipolar elevado, μ=2.45 D.
|
|
|
Anidridos
carboxílicos
Os anidridos de ácidos carboxílicos (ou anidridos carboxílicos) são compostos de fórmula geral R1COOCOR2 . Quando R1=R2 o anidrido diz-se simétrico designando-se misto ou assimétrico quando os dois radicais alquilo são diferentes. A nomenclatura destes compostos consiste em designá-los como anidridos do ou dos ácidos correspondentes. No caso de anidridos simétricos, por exemplo a molécula CH3CO)2O cuja ligação química é descrita na figura 3, o composto é designado anidrido etanóico ou anidrido acético. No caso de anidridos mistos, estes são designados anidrido alcanóico (R1) alcanóico (R2) indicados por ordem alfabética como exemplificado pelo anidrido acético propiónico (ou anidrido etanóico propanóico), CH3C(O)OC(O)CH2CH3, .
|
|
|
Ésteres
Os ésteres são compostos de fórmula genérica R1COOR2 obtidos por reacção de ácidos carboxílicos com álcoois. A nomenclatura de ésteres consiste em identificar o ácido parente, designá-lo pelo anião correspondente substituindo o sufixo óico por ato seguido do nome do radical R2. Por exemplo, o composto CH3COOCH3 é designado acetato ou etanoato de metilo
A ligação química no acetato de metilo é descrita na Fig. 4 que mostra ainda a superfície de densidade electrónica para esta molécula. Devido à presença das ligações C-O a molécula apresenta momento dipolar, μ= 1.73 D
|
|
|
|
|
|